Neurodegenerative
Erkrankungen

Frühdiagnostik ist der Schlüssel zur erfolgreichen Behandlung
Im Kompetenzbereich Biospektroskopie werden u. a. innovative Anwendungen der infrarot (IR)-Spektroskopie entwickelt, um neurodegenerative und neurologische Erkrankungen frühzeitig zu diagnostizieren. Dafür untersuchen wir insbesondere Köperflüssigkeiten wie Blutplasma und Liquor mittels Abgeschwächter Totalreflektions (ATR)-Spektroskopie. Hervorzuheben ist der von uns entwickelte Immuno-Infrarot-Sensor zur Vorhersage der Alzheimer-Erkrankung (Nabers et al, EMBO Molecular Medicine 2018).
Aktuell wird die Alzheimer-Erkrankung erst erkannt, wenn klinische Symptome auftreten. In diesem Krankheitsstadium ist das Gehirn aber bereits irreversibel geschädigt. Für eine erfolgreiche Behandlung ist die Detektion sehr früher Stadien, noch bevor klinische Symptome auftreten, essentiell. Derzeit basiert die klinische Diagnose der Alzheimer-Erkrankung primär auf neuropsychologischen Gutachten. Zusätzlich werden neurochemische Biomarker-Konzentrationen in der Rückenmarksflüssigkeit bestimmt. In Ausnahmefällen wird die nuklearmedizinische Methode der Positronen-Emissions-Tomographie (PET-Scan) zur Detektion amyloider Plaques im Gehirn veranlasst. Letzteres ist ein bildgebendes Verfahren, welches zwar genau ist, aber mit der Verabreichung einer leicht radioaktiven Substanz und hohen Kosten pro Analyse verbunden ist.
Entwicklung eines Bluttest zur Früherkennung von Morbus Alzheimer
Zur Entwicklung von nicht-invasiven, kostengünstigen und sensitiven Diagnosemöglichkeiten werden weltweit enorme Anstrengungen unternommen. Ein Schwerpunkt der Forschungsarbeiten in ProDi richtet sich daher auf die Entwicklung eines Bluttests zur Früherkennung der Alzheimer-Erkrankung. Im Kompetenzbereich Biospektroskopie nutzen wir dafür unsere Expertise im Bereich spektroskopischer Methoden.
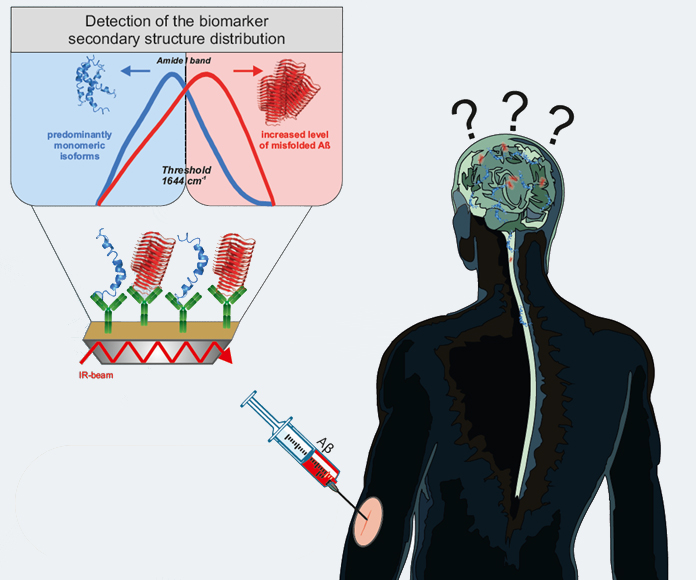
Abb. 1: Alzheimer-Erkrankung: Frühdiagnose durch spektroskopische Analyse von Körperflüssigkeiten mittels des Immuno-Infrarot-Sensors
Ansatzpunkt für Frühdiagnostik im Blut: Amyloid-ß Plaques
Als eine mögliche Ursache der Alzheimer-Erkrankung gilt die Umfaltung des Amyloid-ß (Aß)-Peptids von einem ungeordneten Gemisch aus teils ungefalteten und α–helikalen Sekundärstrukturen hin zu geordneten, zusammengelagerten pathogenen Komplexen vieler Aß-Peptide, den ß-Faltblatt angereicherten Fibrillen. Diese Fibrillen bilden große Aggregate, die für die mit der Alzheimer-Erkrankung assoziierten Plaque-Ablagerungen im Gehirn verantwortlich sind. Der Prozess der Protein-Umfaltung beginnt ca. 15-20 Jahre bevor klinische Symptome auftreten und sich die Erkrankung klinisch manifestiert. Die erhöhte Konzentration von Aß-Fibrillen im Gehirn führt auch zu einer erhöhten Konzentration von Aß-Aggregaten in der Rückenmarksflüssigkeit und im Blut. Das Verhältnis von ungeordneten Aß-Peptiden zu geordneten Aß-Aggregaten bietet uns einen Ansatzpunkt zur spektroskopischen Analyse von Blutplasma aber auch von Rückenmarks- und anderen Körperflüssigkeiten.
Immuno-Infrarot-Sensor: Diagnose durch spektroskopische Körperflüssigkeitsanalyse
Der von uns entwickelte und mit dem Erfinderpreis ausgezeichnete Immuno-Infrarot-Sensor detektiert die Sekundärstrukturverteilung der Aß-Peptide in Körperflüssigkeitsproben. Aus der Sekundärstrukturverteilung wird das Verhältnis von geordneten und ungeordneten Aß-Peptiden abgeleitet, welches eine Differenzierung zwischen Proben von Alzheimer- bzw. nicht-Alzheimer-Erkrankten-Patienten erlaubt. Zunächst haben wir das Verfahren in verschiedenen Studien zur Analyse von Rückenmarksflüssigkeit (Liquor) eingesetzt. Dabei erzielten wir eine Sensitivität von 94 % und eine Spezifität von 88 % bei der Unterscheidung von Alzheimer-Patienten und Kontroll-Personen (Nabers et al Journal of Biophotonics 2016). Das bedeutet, dass wir 94 % der Patienten mit einer Alzheimer-Erkrankung sicher als krank und 88 % der tatsächlich gesunden Patienten als gesund erfasst haben.

Abb. 2: Anschließen einer Blutplasmaprobe an den Immuno-Infrarot-Sensor.
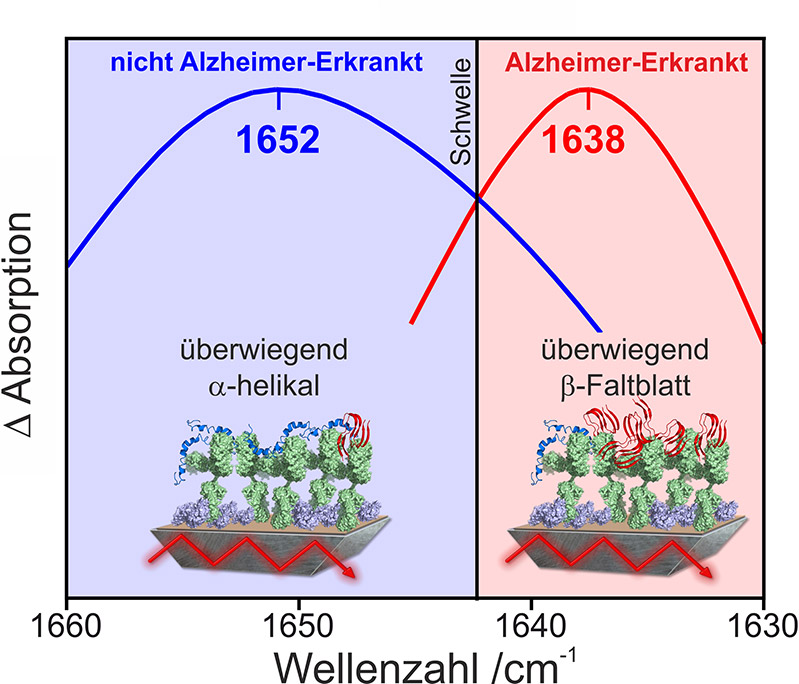
Abb. 3: Spektrale Unterscheidung von Alzheimer- und nicht Alzheimer-erkrankten Patienten.
Frühdiagnose durch spektroskopische Analyse von Blutplasma
Da die Entnahme von Rückenmarksflüssigkeit risikobehaftet und schmerzhaft ist, haben wir unseren Diagnoseansatz auf die spektroskopische Analyse von Blutplasma ausgeweitet. Blutplasma wird durch den minimal-invasiven Eingriff einer Blutabnahme gewonnen. Bei der Analyse von Blutplasma konnten wir im ersten Schritt eine Sensitivität von 75 % und eine Spezifität von 88 % in gut gesicherten Alzheimer-Fällen erzielen (Nabers et al Analytical Chemistry 179). Im nächsten Schritt haben wir das frühdiagnostische Potenzial des Immuno-Infrarot-Sensors anhand von Langzeitstudien belegt. Mit unserem Diagnoseverfahren erzielten wir eine präklinische Detektion der Alzheimer-Erkrankung in Blutplasma mit einer Sensitivität von 71 % und Spezifität von 91 %. Unsere Studie belegt, dass der Immuno-Infrarot-Sensor die Alzheimer-Erkrankung im Blutplasma bereits 8-14 Jahre vor dem Auftreten von klinischen Symptomen – und somit in einem sehr frühen Krankheitsstadium – nachweist (Nabers et al EMBO Molecular Medicine 2018). Kombinieren wir unseren Struktur-Biomarker zur Vorhersage künftiger kognitiver Einschränkungen mit dem genetischen Risiko (APOE-Status) hat unser Verfahren in 86 % aller Fälle präzise vorausgesagt, welche Studienteilnehmer (ESTHER Studie Heidelberg) im Laufe von 8-14 Jahren nach Probennahme Alzheimer-Symptome entwickelt haben (Stocker et al Alzheimer’s & Dementia 2019.
Eine Basis für Diagnosetests verschiedener neurologischer Erkrankungen
Neben dem Aß-Peptid gibt es weitere Proteine, deren Veränderung der Sekundärstruktur mit Krankheiten in Verbindung gebracht wird. Diese Proteine werden als Biomarker bezeichnet. Das Tau-Protein ist zum Beispiel ein weiterer Biomarker für die Alzheimer-Erkrankung. Weitere Struktur-veränderte Proteine, die als Biomarker fungieren, sind alpha-Synuklein oder Huntingtin, die mit Parkinsonsymptomen bzw. Huntington assoziiert werden. Die Analyse der Sekundärstruktur von Proteinen mit dem Immuno-Infrarot-Sensor bietet somit auch die Möglichkeit, weitere Erkrankungen näher zu untersuchen. Ein sicherer und einfacher Bluttest zur Frühdiagnose ist ein großer Schritt in Richtung Therapie und Vorsorge von neurodegenerativen Erkrankungen.
Presse
Presseinformationen
Pressespiegel
Drittmittelförderung

111.08.03.05-133974
Validierung und Standardisierung des Workflows zur Proteindiagnostik

Correlation between Aβ42 decrease and misfolding in blood
PURE – Protein Research Unit Ruhr within Europe
Validierung Marker-freier Imaging Verfahren und neu identifizierter Biomarker unter Nutzung des PURE-Konsortium